La lucha contra el alzhéimer ha dado un giro relevante en Europa. La Comisión Europea ha autorizado el uso de lecanemab, un anticuerpo monoclonal dirigido contra el beta-amiloide, para personas con deterioro cognitivo leve o demencia leve por enfermedad de Alzheimer, bajo condiciones estrictas de selección y seguimiento. La noticia abre una nueva etapa: no es una cura, pero sí el primer tratamiento en la UE que apunta a modificar el curso de la enfermedad en fases tempranas.
La autorización europea llega tras la evaluación de la Agencia Europea de Medicamentos (EMA) y se apoya en ensayos clínicos que mostraron una ralentización modesta del deterioro en pacientes cuidadosamente seleccionados. En la práctica, el fármaco se dirige a un perfil muy concreto: personas con alzhéimer en fase inicial, con evidencia de acumulación de amiloide en el cerebro (confirmada mediante PET amiloide o biomarcadores en líquido cefalorraquídeo) y con criterios de seguridad que reducen el riesgo de efectos adversos.
“Es un paso importante porque, por primera vez en Europa, disponemos de una terapia que no solo trata síntomas, sino que actúa sobre una diana biológica de la enfermedad”, explica la neuróloga María Jesús Carrasco, especialista en trastornos cognitivos en un hospital público madrileño. “Ahora el reto es organizar el diagnóstico temprano y el seguimiento, porque el tratamiento exige un circuito asistencial muy estructurado”, añade.
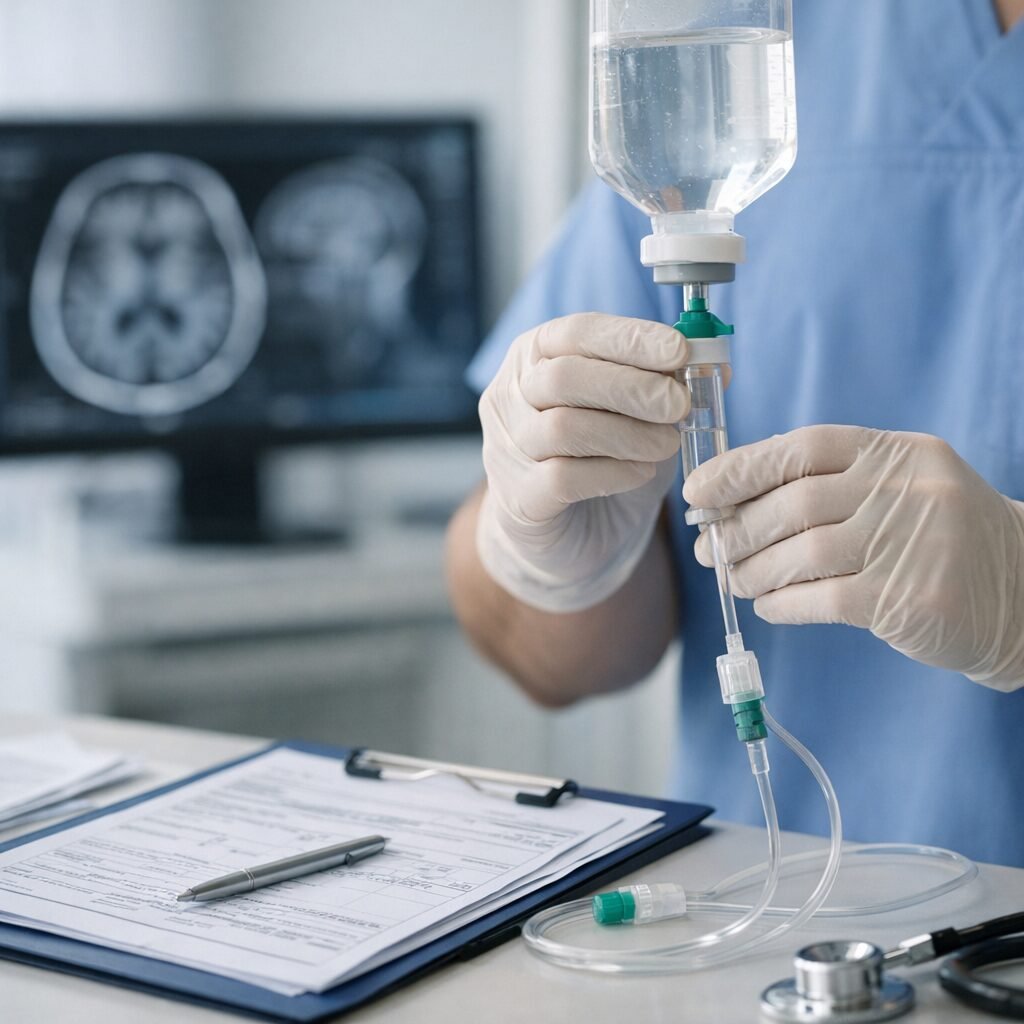
El punto clave es entender qué aporta (y qué no). Lecanemab se administra por infusión intravenosa y su objetivo es reducir placas de beta-amiloide. En los estudios, la diferencia frente a placebo se tradujo en una desaceleración del declive funcional y cognitivo, pero no revierte los síntomas ni detiene por completo la progresión. Por ello, los expertos insisten en ajustar expectativas: el beneficio, aunque clínicamente relevante para algunos pacientes, es limitado y depende de iniciar el tratamiento pronto.
La otra cara de la moneda es la seguridad. El principal riesgo asociado a este tipo de terapias antiamiloide son las llamadas ARIA (anomalías de imagen relacionadas con amiloide), que incluyen edema cerebral (ARIA-E) y microhemorragias (ARIA-H). Por ese motivo, los protocolos europeos exigen resonancias magnéticas periódicas y una selección cuidadosa, especialmente en personas con factores de riesgo de sangrado cerebral o que toman determinados anticoagulantes. También se considera relevante el genotipo APOE ε4, asociado a mayor probabilidad de ARIA, motivo por el que en muchos centros se plantea el test genético como parte de la evaluación clínica, siempre con asesoramiento.
“La aprobación no significa tratamiento para todos: significa tratamiento para quienes cumplan criterios y puedan ser monitorizados con seguridad”, subraya Pablo Martínez-Lage, neurólogo y portavoz habitual en iniciativas de divulgación sobre demencias. “Además, obliga a reforzar la capacidad diagnóstica: sin biomarcadores no hay indicación”, apunta.
En España, el impacto dependerá de cómo se articule su incorporación al Sistema Nacional de Salud. Tras la autorización europea, el siguiente paso es la evaluación de financiación y precio y, posteriormente, la implementación en cada comunidad autónoma. A nivel asistencial, el desafío es doble: por un lado, ampliar el acceso a pruebas que confirmen la patología de Alzheimer (PET o biomarcadores); por otro, crear itinerarios de monitorización con neurología, radiología y enfermería especializada, incluyendo resonancias y manejo de efectos adversos. Esto podría acelerar la transformación de las consultas de memoria hacia modelos más similares a los de oncología o enfermedades autoinmunes, donde el seguimiento estrecho es la norma.
La noticia también reabre el debate sobre el diagnóstico precoz. Muchos casos se detectan tarde, cuando ya existe un deterioro significativo. Identificar antes a las personas candidatas implica mejorar la formación en atención primaria, acortar tiempos de derivación y normalizar el acceso a unidades de memoria. En paralelo, se refuerza un mensaje que a menudo se pierde en el ruido de los avances farmacológicos: la prevención y el control de factores de riesgo siguen siendo esenciales. La evidencia acumulada asocia un menor riesgo de demencia con hábitos como el ejercicio regular, la dieta saludable (por ejemplo, patrón mediterráneo), el control de la hipertensión, el abordaje de la pérdida auditiva, el sueño adecuado y la reducción del aislamiento social.
El cierre, por tanto, es realista: la aprobación de lecanemab marca un hito, pero no sustituye la necesidad de políticas de salud pública ni de apoyo a cuidadores. Si se implementa con criterios claros, puede ofrecer tiempo valioso en una etapa en la que cada mes cuenta para mantener autonomía. La innovación llega, pero su verdadero impacto dependerá de que el sistema sea capaz de diagnosticar antes, tratar mejor y acompañar más.