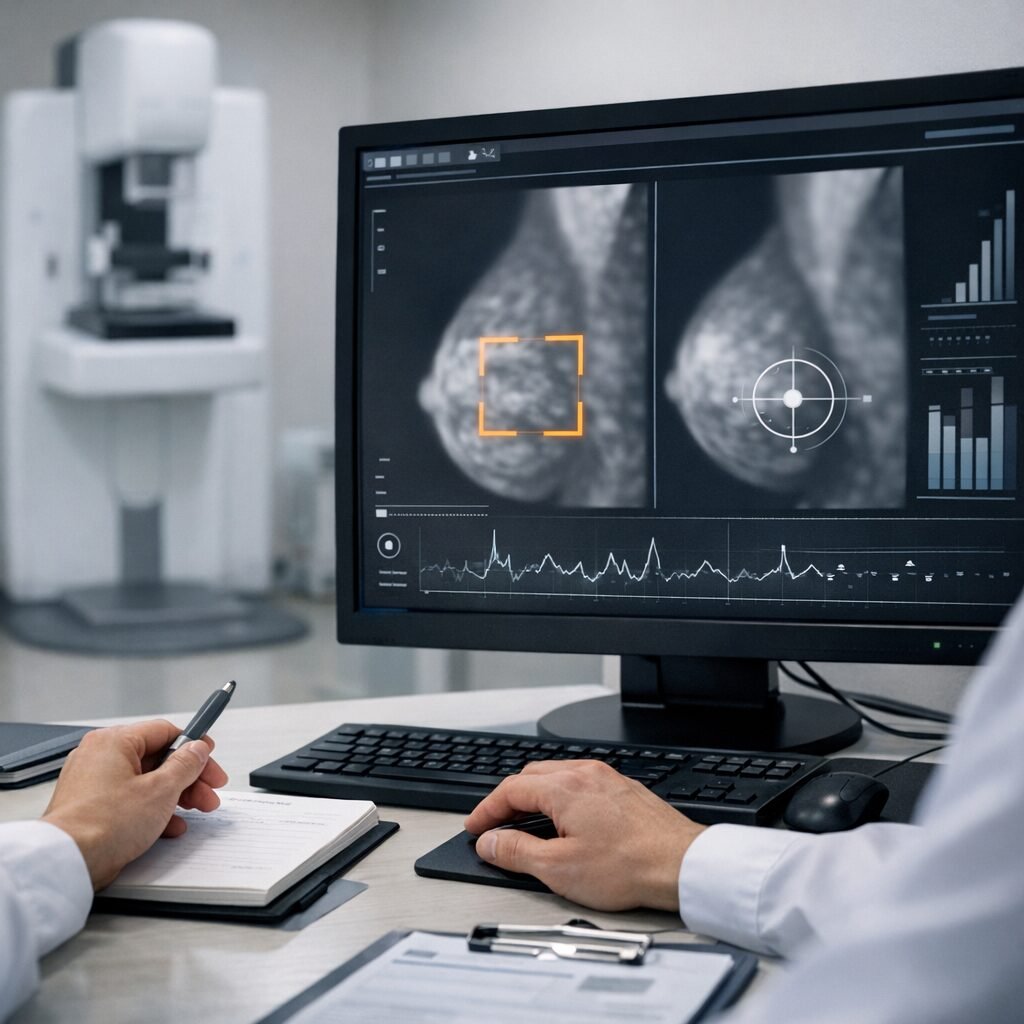
La promesa de la inteligencia artificial en medicina lleva años sonando a futuro, pero en 2026 empieza a traducirse en cambios muy concretos en un terreno sensible: el cribado del cáncer de mama. En los últimos meses, varios servicios de radiodiagnóstico en Europa han acelerado la incorporación de herramientas de apoyo basadas en IA para priorizar estudios, reducir cargas de trabajo y, sobre todo, ayudar a detectar lesiones sutiles que pueden pasar desapercibidas en una primera lectura.
La clave no es “sustituir” al especialista, sino reforzar un proceso que ya de por sí es exigente. La mamografía es una prueba eficaz para reducir mortalidad cuando está bien implementada, pero su interpretación tiene límites: la densidad mamaria, las microcalcificaciones o la superposición de tejidos pueden complicar la lectura. En este contexto, los sistemas de IA actúan como un segundo par de ojos: analizan patrones en la imagen, señalan áreas sospechosas y ofrecen una puntuación de riesgo que el radiólogo contrasta con su criterio clínico.
En Europa, el debate se ha intensificado a raíz de la evidencia generada en programas de cribado poblacional. Un hito relevante fue el ensayo MASAI (Mammography Screening with Artificial Intelligence), realizado en Suecia y publicado en The Lancet Oncology (2023). Este estudio evaluó el uso de IA en un entorno real de cribado y observó que el apoyo algorítmico permitió aumentar la detección de cáncer y, al mismo tiempo, reducir la carga de lectura de los radiólogos, sin un incremento significativo de falsos positivos que disparara las biopsias innecesarias. No es una varita mágica, pero sí una señal de que la tecnología puede aportar valor cuando se integra con protocolos y auditorías.
La presión asistencial también empuja. España mantiene programas de cribado organizados por comunidades autónomas, generalmente dirigidos a mujeres de 50 a 69 años (con variaciones), y afronta un reto compartido con otros países: cada vez más pruebas, más complejidad y plantillas limitadas. En radiología, la doble lectura (dos profesionales revisan la misma mamografía) mejora la sensibilidad, pero consume tiempo y recursos. La IA abre la puerta a modelos híbridos: por ejemplo, usar el algoritmo para identificar estudios claramente normales y reservar la doble lectura humana para los casos más dudosos, siempre con medidas de seguridad y validación local.
“La IA no decide por la paciente; ayuda a que el radiólogo no pase por alto hallazgos sutiles y a organizar mejor el flujo de trabajo”, explica la doctora Laura Sánchez, radióloga en un hospital público de Madrid, en declaraciones a este medio. “Pero su implementación exige formación, control de calidad y revisar el rendimiento en nuestra población: no basta con instalar un software”.
El encaje regulatorio y ético es otro punto crítico. En la Unión Europea, el Reglamento de Productos Sanitarios (MDR) y el nuevo marco de la Ley de IA marcan obligaciones crecientes para sistemas de alto riesgo en salud: trazabilidad, gestión de riesgos, supervisión humana y transparencia. La pregunta práctica para los centros es cómo convertir esos principios en rutinas: auditorías periódicas, registro de incidencias, evaluación de sesgos y protocolos claros ante discrepancias entre IA y especialista.
¿Y qué significa esto para las pacientes? En el mejor de los escenarios, se traduce en diagnósticos más tempranos y procesos más ágiles. Un cáncer detectado en fases iniciales suele permitir tratamientos menos agresivos y mejores tasas de supervivencia. Sin embargo, la comunicación sigue siendo esencial: la IA puede aumentar la detección, pero también puede elevar la tasa de “recalls” (llamadas para pruebas adicionales) si no se calibra bien, lo que genera ansiedad. Por eso, los expertos insisten en medir no solo la sensibilidad, sino el impacto global: falsos positivos, tiempos de espera, número de biopsias, y resultados a largo plazo.
“Lo importante es que el despliegue sea responsable: validación clínica, evaluación continua y transparencia con la ciudadanía”, señala María José Roldán, especialista en salud pública y evaluación de tecnologías sanitarias. “La innovación tiene sentido si mejora resultados y experiencia, no solo si añade complejidad”.
La otra cara del avance es la calidad de los datos. Los algoritmos aprenden de grandes volúmenes de imágenes etiquetadas; si esos datos no representan bien la diversidad (edad, densidad mamaria, equipos de imagen, prevalencia real), el rendimiento puede variar. Por eso, muchos hospitales están apostando por pruebas piloto y comparaciones internas antes de extender el sistema a todo el programa. También crece el interés por herramientas que expliquen mejor por qué señalan una zona, para facilitar la revisión clínica y reducir la “caja negra”.
En resumen, la IA aplicada al cribado mamográfico se está consolidando como una herramienta útil, pero su éxito dependerá menos del algoritmo y más del ecosistema: profesionales formados, protocolos robustos, supervisión humana y evaluación real en cada servicio. Para las pacientes, el mensaje es doble: el cribado sigue siendo una de las estrategias más eficaces para detectar cáncer de mama a tiempo, y la tecnología puede mejorar su precisión, siempre que se use con rigor, prudencia y transparencia.