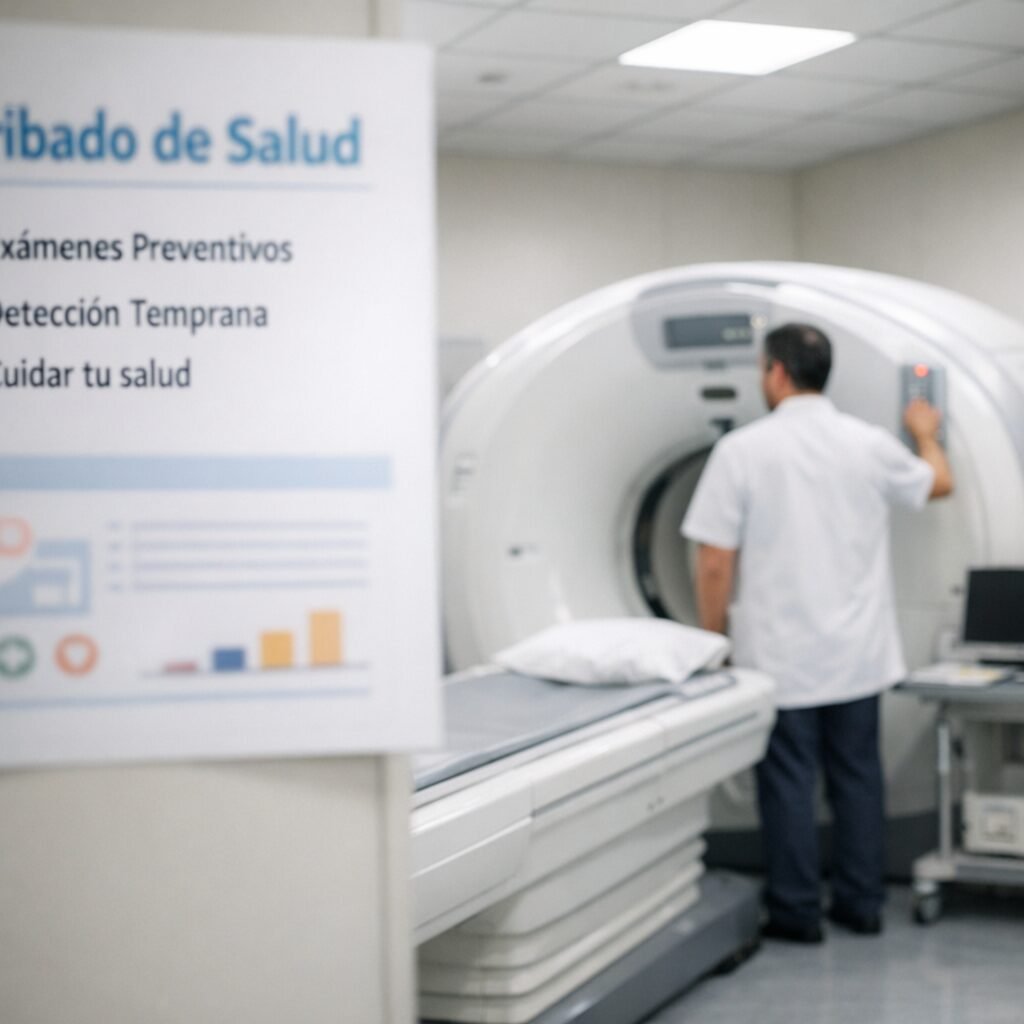
Durante años, el cáncer de pulmón ha sido el “gran asesino silencioso” de la oncología: suele dar la cara tarde y, cuando lo hace, las opciones se estrechan. La buena noticia es que el diagnóstico precoz ya no es una promesa lejana. El TAC de baja dosis (LDCT), una prueba rápida y con menor radiación que un TAC convencional, está consolidándose como la herramienta más eficaz para detectar tumores en fases iniciales en personas con alto riesgo. En España, su implantación avanza, pero de forma desigual y con retos organizativos por resolver.
La evidencia científica que respalda el cribado es sólida. Grandes ensayos clínicos como el National Lung Screening Trial (NLST) en Estados Unidos y el estudio NELSON en Europa demostraron que el cribado con LDCT en población seleccionada reduce la mortalidad por cáncer de pulmón frente a no cribar. A partir de esos resultados, las recomendaciones internacionales han ido convergiendo: priorizar a personas de 50 a 80 años (el rango exacto depende de la guía) con un historial de tabaquismo importante —medido en “paquetes-año”— y, en algunos casos, exfumadores recientes.
El impulso más reciente en el marco europeo ha llegado con el Plan Europeo de Lucha contra el Cáncer y las recomendaciones de la UE para reforzar programas de detección precoz. Aunque el cribado de pulmón no está tan desplegado como el de mama o colon, varios países han acelerado pilotos y escalados regionales. En España, el debate ya no es tanto si funciona, sino cómo implementarlo de forma segura, equitativa y coste-efectiva.
“El TAC de baja dosis permite detectar nódulos pequeños cuando todavía son tratables con cirugía o radioterapia de alta precisión. Pero el cribado no es solo hacer una prueba: requiere circuitos claros para el seguimiento, equipos entrenados y protocolos para reducir falsos positivos”, señala la doctora Isabel García, neumóloga en un hospital público madrileño. Su advertencia apunta al principal desafío: el cribado mal organizado puede generar ansiedad, pruebas invasivas innecesarias o saturación de radiología.
Los beneficios, sin embargo, pueden ser significativos cuando el programa está bien diseñado. Detectar un tumor en estadio I o II cambia radicalmente el pronóstico. Además, el cribado abre una puerta estratégica: convertir cada cita en una intervención de salud pública. “El momento del cribado es una oportunidad de oro para ofrecer apoyo real para dejar de fumar. Si no integramos la cesación tabáquica, perdemos la mitad del impacto”, explica Javier López, responsable de una unidad de tabaquismo. La literatura es consistente: combinar cribado con programas de abandono del tabaco mejora resultados y reduce riesgos a medio plazo.
¿Quién debería planteárselo? Las guías internacionales suelen centrarse en personas con alto riesgo por tabaquismo (por ejemplo, 20 paquetes-año o más, y fumadores actuales o exfumadores que dejaron el tabaco en los últimos 15 años). No es una prueba para población general: en personas de bajo riesgo, los daños potenciales (falsos positivos, radiación acumulada, hallazgos incidentales) pueden superar los beneficios. En consulta, la decisión debe ser compartida, valorando edad, comorbilidades y capacidad de someterse a tratamiento si se detecta un tumor.
También hay matices importantes sobre seguridad. La radiación del LDCT es baja, pero no es cero; por eso se recomienda periodicidad anual solo en quienes realmente se benefician. Otro punto crítico es la lectura de imágenes: el uso de sistemas estandarizados (como categorías de nódulos y algoritmos de seguimiento) reduce variabilidad y evita intervenciones precipitadas. En paralelo, la inteligencia artificial está empezando a utilizarse como apoyo para detectar nódulos y priorizar estudios, aunque su papel debe ser complementario y validado en cada entorno clínico.
En España, el avance se apoya en experiencias locales, proyectos piloto y la creciente coordinación entre neumología, radiología, atención primaria y oncología. Aun así, persisten barreras: listas de espera, falta de circuitos homogéneos entre comunidades, y la necesidad de definir criterios comunes de inclusión y seguimiento. La equidad es clave: el cáncer de pulmón se asocia con mayor carga en grupos socioeconómicos más vulnerables, donde el acceso a prevención y abandono del tabaco suele ser más difícil.
El cierre del círculo pasa por asumir que el cribado no sustituye a la prevención: no fumar sigue siendo la medida más eficaz para reducir el riesgo. Pero para quienes han fumado durante décadas, la detección precoz puede ser la diferencia entre una intervención curativa y un diagnóstico tardío. La pregunta que se abre ahora es de política sanitaria: si la evidencia ya está sobre la mesa, el siguiente paso es convertirla en un programa estable, bien financiado y con garantías, para que el código postal no decida quién llega a tiempo.