Durante años, el Alzheimer ha sido el ejemplo más duro de una promesa médica que parecía siempre a punto de cumplirse… y nunca llegaba. Esta semana, Europa da un paso relevante: la Agencia Europea de Medicamentos (EMA) ha recomendado autorizar lecanemab, el primer fármaco en la Unión Europea con evidencia de ralentización del deterioro cognitivo en personas con enfermedad de Alzheimer en fases iniciales. No es una cura, pero sí un cambio de paradigma que abre nuevas preguntas sobre diagnóstico precoz, seguimiento y acceso.
La recomendación de la EMA se refiere a un uso concreto: pacientes con deterioro cognitivo leve o demencia leve por Alzheimer, y con confirmación de la patología amiloide (habitualmente mediante PET o biomarcadores en líquido cefalorraquídeo, y cada vez más con pruebas sanguíneas en evaluación clínica). En la práctica, significa que el tratamiento se plantea para un perfil de persona que todavía mantiene buena parte de su autonomía, pero en quien ya se ha identificado el proceso neurodegenerativo.
Lecanemab es un anticuerpo monoclonal dirigido contra el beta-amiloide. Su objetivo es reducir las placas amiloides en el cerebro, una de las señas biológicas de la enfermedad. La evidencia principal procede del ensayo clínico de fase 3 CLARITY-AD, publicado en 2022 en The New England Journal of Medicine, que mostró una reducción del 27% en el declive clínico a los 18 meses frente a placebo en una escala compuesta de función cognitiva y diaria en personas con Alzheimer temprano. Traducido a la vida real: el beneficio es moderado, pero medible, y requiere iniciar el tratamiento pronto.
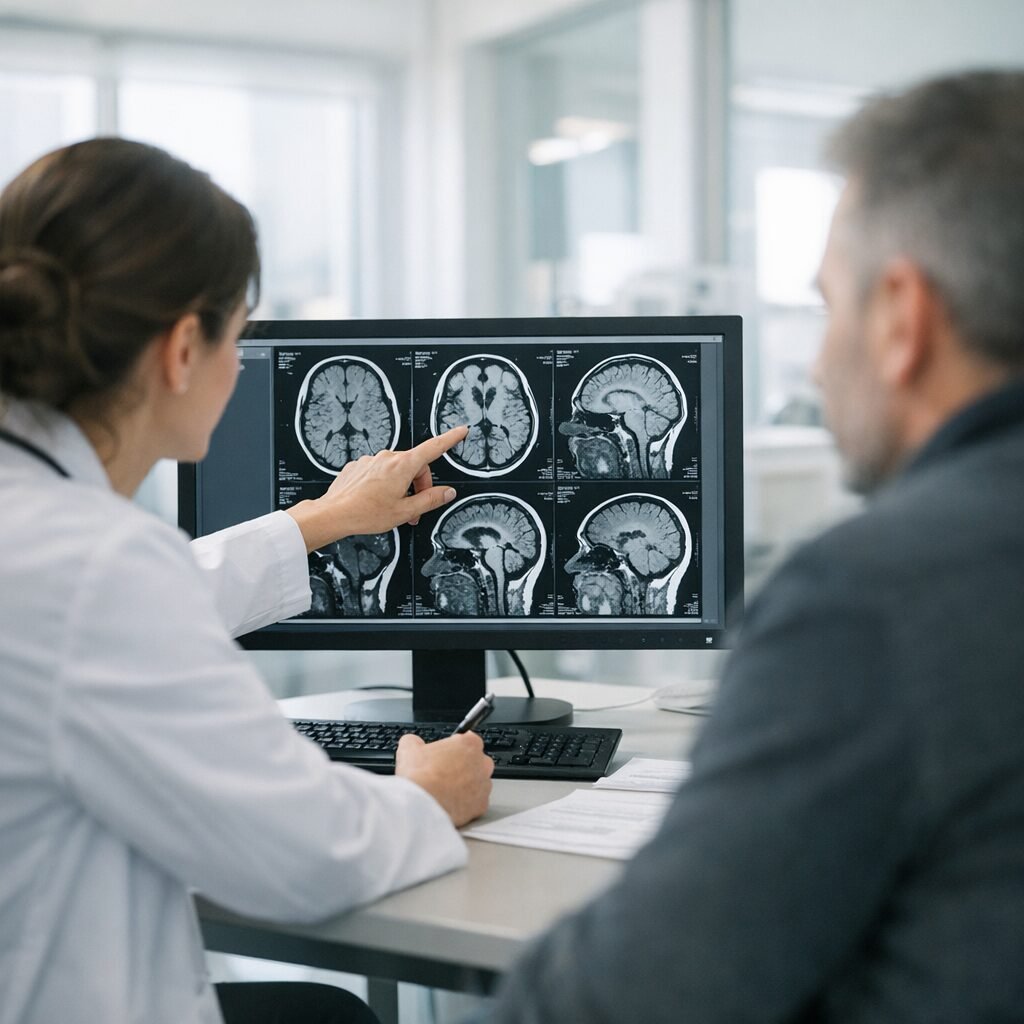
El avance llega acompañado de un aviso importante: el efecto no está exento de riesgos. Uno de los principales es la aparición de ARIA (anomalías de imagen relacionadas con amiloide), que puede manifestarse como edema cerebral o microhemorragias detectables en resonancia magnética. Aunque muchos casos son asintomáticos, algunos pueden producir cefalea, confusión o síntomas neurológicos. Por eso, el uso del fármaco exige protocolos de seguridad y monitorización con resonancias periódicas, especialmente al inicio.
“Estamos ante un paso adelante real, pero no ante una solución definitiva. El mayor reto será identificar a los pacientes adecuados y garantizar un seguimiento seguro”, explica la neuróloga Ana Martínez, especialista en demencias de un hospital público de Madrid. “Esto obliga a reforzar circuitos de diagnóstico precoz, biomarcadores y acceso a neuroimagen, que hoy son desiguales según la comunidad autónoma”.
La recomendación europea también reabre el debate sobre cómo se diagnostica el Alzheimer. Hasta hace poco, el diagnóstico era principalmente clínico; hoy, los biomarcadores permiten confirmar el proceso biológico incluso antes de la demencia. En España, unidades de memoria y servicios de neurología han ido incorporando PET amiloide, punciones lumbares y, en algunos centros, pruebas sanguíneas en contextos controlados. Aun así, el acceso sigue siendo limitado y la lista de espera puede ser larga, un obstáculo cuando el beneficio del tratamiento depende de actuar pronto.
Desde el punto de vista de salud pública, el impacto potencial es grande, pero no inmediato. Según la OMS, la demencia afecta a decenas de millones de personas en el mundo, y el Alzheimer es la causa más frecuente. En España, las estimaciones sitúan el número de personas con demencia en torno a cientos de miles, con un peso creciente por el envejecimiento poblacional. Sin embargo, el tratamiento aprobado se dirige a un subconjunto: quienes están en fases iniciales y cumplen criterios biológicos y clínicos estrictos.
“Es una innovación que empuja al sistema a modernizarse: no solo es el fármaco, es todo lo que lo rodea —diagnóstico, resonancias, equipos multidisciplinares, información al paciente—”, señala Javier Sanz, farmacéutico hospitalario y miembro de una comisión de evaluación de medicamentos. “La clave será equilibrar el potencial beneficio con el riesgo de efectos adversos y con la capacidad real de los hospitales para monitorizar”.
Además, el contexto internacional muestra que la historia no es lineal. En Estados Unidos, la FDA autorizó lecanemab en 2023, y desde entonces se ha debatido intensamente sobre criterios de uso, cobertura y seguridad. En Europa, la evaluación ha sido especialmente cauta, y la recomendación de autorización llega acompañada de condiciones y de la necesidad de planes de gestión de riesgos.
Para las familias, la noticia puede generar expectativas altas. Los expertos insisten en matizar: el tratamiento no revierte el daño ya producido y su objetivo es retrasar el avance, no detenerlo. Aun así, incluso una ralentización puede suponer meses de mejor funcionamiento y más tiempo de autonomía, un valor enorme en una enfermedad que afecta a la identidad, la independencia y la vida cotidiana.
El cierre, por tanto, es doble: esperanza y responsabilidad. Esperanza porque, por primera vez en Europa, un fármaco para Alzheimer temprano muestra un efecto clínico consistente sobre la progresión. Responsabilidad porque el éxito dependerá de diagnosticar antes, tratar mejor y vigilar con rigor. El verdadero cambio no será solo tener un nuevo medicamento, sino construir el sistema que permita usarlo con seguridad y equidad.