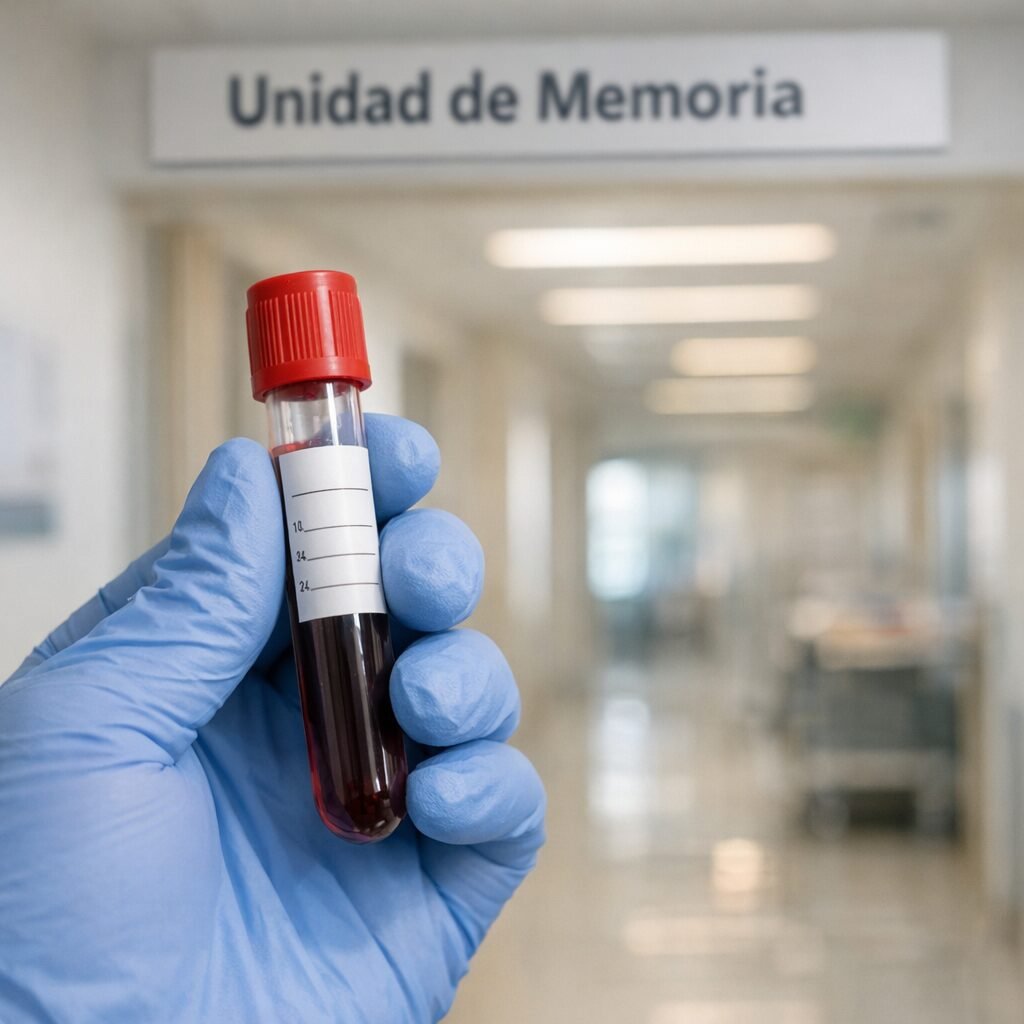
La idea de confirmar el alzhéimer con un simple análisis de sangre, sin depender de pruebas complejas y costosas, está dejando de ser ciencia ficción. En los últimos meses, varios hospitales y laboratorios europeos han acelerado la validación clínica de biomarcadores en sangre capaces de identificar con gran precisión la presencia de patología amiloide, un sello biológico de la enfermedad. El cambio promete acortar años de incertidumbre para miles de personas con quejas de memoria y, al mismo tiempo, abre un debate sanitario: cómo usar esta información de forma responsable cuando todavía no existe una cura definitiva.
Hasta ahora, el diagnóstico biológico del alzhéimer se apoyaba sobre todo en dos herramientas: la punción lumbar para analizar líquido cefalorraquídeo y la tomografía por emisión de positrones (PET) para visualizar depósitos de amiloide en el cerebro. Ambas aportan un alto valor clínico, pero no siempre son accesibles: la PET es cara y requiere equipamiento especializado; la punción lumbar, aunque segura en manos expertas, puede generar rechazo y no está disponible en todos los centros. En ese contexto, la sangre se ha convertido en el gran objetivo por su potencial para democratizar el diagnóstico y facilitar el seguimiento.
Los biomarcadores más prometedores miden proteínas relacionadas con la neurodegeneración y la acumulación de amiloide. Entre ellos destacan el p-tau217 y el p-tau181 (formas fosforiladas de la proteína tau), así como la relación Aβ42/Aβ40 (beta amiloide). En estudios recientes publicados en revistas biomédicas de referencia, estos marcadores han mostrado una capacidad elevada para predecir positividad amiloide respecto a PET o líquido cefalorraquídeo, especialmente cuando se aplican en personas con deterioro cognitivo leve o síntomas iniciales en unidades de memoria. La evidencia también apunta a que algunos de estos marcadores se correlacionan con la progresión clínica, lo que podría ayudar a monitorizar la enfermedad.
La gran pregunta no es solo si funcionan, sino cómo y a quién se deben ofrecer. “Un test sanguíneo puede reducir tiempos y evitar pruebas innecesarias, pero no sustituye la valoración clínica. El riesgo está en banalizar un resultado sin contexto”, explica la neuróloga Ana Beltrán, especialista en trastornos cognitivos en un hospital público español. La experta subraya que el alzhéimer no se diagnostica por un biomarcador aislado: historia clínica, exploración neurológica, evaluación neuropsicológica y, en ocasiones, neuroimagen siguen siendo piezas clave.
En paralelo, el interés por la sangre se ha disparado por un motivo práctico: la llegada de terapias modificadoras de la enfermedad dirigidas contra el amiloide. Estos tratamientos —aprobados en algunos países y en evaluación o despliegue progresivo en otros— requieren seleccionar a pacientes en fases tempranas y confirmar la presencia de amiloide. Un análisis de sangre fiable podría actuar como prueba de cribado para decidir quién necesita una PET o una punción lumbar, optimizando recursos y reduciendo listas de espera. “Si la sangre permite filtrar con precisión, podemos reservar las pruebas más complejas para los casos en los que realmente aportan valor”, señala Javier Molina, bioquímico clínico vinculado a un laboratorio hospitalario, que recuerda que la estandarización analítica y los controles de calidad serán determinantes.
Sin embargo, el salto a la práctica clínica exige cautela. Los biomarcadores pueden variar según la técnica utilizada, la plataforma de medición y el punto de corte elegido. Además, la interpretación cambia según la población: no es lo mismo estudiar a pacientes ya derivados a una consulta de memoria que aplicar el test en población general. Los expertos advierten de que usar estas pruebas como “screening” masivo podría generar falsos positivos, ansiedad y un consumo innecesario de recursos. También existe el riesgo contrario: falsos negativos que retrasen la atención especializada.
Otro aspecto sensible es el impacto emocional y ético. Conocer un resultado compatible con patología amiloide puede ayudar a planificar, acceder antes a apoyos y participar en ensayos clínicos, pero también implica afrontar incertidumbre: algunas personas con amiloide pueden tardar años en desarrollar síntomas relevantes. Por eso, los protocolos recomiendan que la información se entregue con asesoramiento clínico y un plan de seguimiento, evitando que el test se convierta en un producto de consumo sin acompañamiento profesional.
En España, el despliegue dependerá de la evaluación por parte de sociedades científicas, la disponibilidad en laboratorios acreditados y la incorporación a circuitos asistenciales. Los especialistas coinciden en que la primera puerta de entrada razonable son las unidades de memoria y neurología, donde el test podría integrarse como herramienta de apoyo para decidir el siguiente paso diagnóstico. A medio plazo, podría extenderse a atención primaria para acelerar derivaciones, siempre con criterios claros, formación y rutas asistenciales bien definidas.
El avance es real y tangible: por primera vez, la medicina se acerca a un escenario en el que una extracción de sangre ayude a orientar el diagnóstico del alzhéimer con rapidez. Pero el verdadero éxito no será solo tecnológico. Será conseguir que esta innovación se traduzca en diagnósticos más tempranos, equitativos y bien acompañados, sin generar ruido ni miedo. Para pacientes y familias, la promesa es sencilla: menos espera, más claridad y mejores decisiones a tiempo.